Mách bạn các “bẫy” thường gặp trong đề thi THPT Quốc gia môn Hóa học
Trong đề thi THPT Quốc gia, các câu hỏi sẽ có các mức độ từ dễ đến khó khác nhau. Tuy nhiên, có những câu hỏi mặc dù không quá khó nhưng nhiều thí sinh vẫn làm sai. Bởi trong quá trình làm bài thi, các thí sinh không để ý đến những cái "bẫy" trong câu hỏi. Để giúp các bạn không bị mất điểm một cách đáng tiếc, chúng tôi đã tổng hợp một số loại “bẫy” thường gặp trong đề thi môn Hóa học.
- Tổng hợp một số đề bài và dàn ý chi tiết các bài văn liên hệ tác phẩm văn học ôn thi THPT
- Một số đề thi thử tốt nghiệp THPT môn Hóa học (có đáp án)
- Kinh nghiệm ôn tập và làm bài thi trắc nghiệm môn Giáo dục công dân đạt điểm cao
Cấu trúc đề thi THPT Quốc gia môn Hóa học
Theo đề thi tham khảo môn Hóa học của Bộ GD&ĐT công bố, tỉ lệ câu hỏi thuộc chương trình Hóa học 11 là 10%, còn lại 90% là các câu hỏi thuộc chương trình lớp 12, không có câu hỏi chỉ thuộc chương trình lớp 10.
Trong đó các câu hỏi lớp 11 tập trung chủ yếu vào chương sự điện li, nitơ, photpho, đại cương hóa hữu cơ và chủ yếu thuộc các cấp độ Nhận biết/thông hiểu và vận dụng thấp.
Các câu hỏi vận dụng cao để phân loại học sinh vẫn nằm trong các chuyên đề lớn như Este, lipit, tổng hợp hóa học vô cơ, tổng hợp hóa học hữu cơ, kim loại kiềm, kiềm thổ, nhôm và hợp chất thuộc chương trình Hóa học 12.
➤TUYỂN SINH CAO ĐẲNG Y DƯỢC CHÍNH QUY XÉT TỐT NGHIỆP CẤP 3![]()
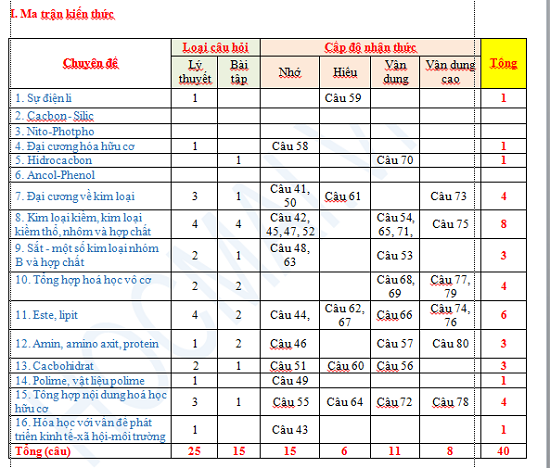
Ma trận kiến thức đề thi THPT quốc gia môn Hóa học năm 2019 của Bộ GD&ĐT
Các “bẫy” thường gặp trong đề thi môn Hóa học
Bẫy về kiến thức lý thuyết
Chẳng hạn: bẫy phản ứng của sắt đơn chất (Fe) với chất oxy hóa mạnh như HNO3, H2SO4 đặc nóng. Nhiều học sinh vội vàng thường kết luận trong trường hợp này Fe sẽ tạo ion Fe3+, nhưng thực tế nếu Fe dư, phản ứng hoàn toàn thì sản phẩm cuối cùng là Fe2+. Hoặc nếu các chất đều hết, có thể tạo cả hai dạng ion sắt.
=> Thí sinh nên học thật kỹ lý thuyết để tránh nhầm lẫn trong những câu hỏi thuộc phần kiến thức trọng tâm.
Bẫy về ngôn ngữ của đề
Chẳng hạn: Xà phòng hóa hết a gam etylaxetat bằng 120ml dung dịch NaOH 2M, sau phản ứng cô cạn dung dịch được 18 gam chất rắn. Tìm giá trị của a?
Nếu hiểu không kỹ, học sinh sẽ dễ lầm đề là lượng NaOH phản ứng vừa đủ rồi tính theo số mol của NaOH ban đầu, hoặc tưởng rằng 18 gam chất rắn là muối natri axetat rồi tính theo số mol của muối. Thực chất ở đây chỉ este hết còn NaOH có thể còn dư và chất rắn có thể chứa NaOH.
Bởi vậy, thí sinh cần đặt ẩn số cho số mol của este, lập phương trình phản ứng xà phòng hóa và giải theo số mol của este.
=> Đọc kỹ đề, suy nghĩ kỹ đề để hiểu rõ ngôn ngữ trong đề
Bẫy ở dạng bài vận dụng cao
Ở những bài tập có sự hiện diện của 3 kim loại Mg , Al , Zn tác dụng với HNO3 hoặc H+ và NO3 –, do tính khử tương đối mạnh của những kim loại này nên khả năng xuất hiện NH4NO3 là rất cao (99,99% trong các bài tập hiện nay).
Trừ khi đề bài cho thêm dữ kiện chất khí nào là sản phẩm khử duy nhất của N+5, nếu không chúng ta phải hết sức cảnh giác có sự xuất hiện của NH4NO3. Đây chính là bẫy của rất nhiều bài toán, nếu học sinh bỏ qua vấn đề này sẽ dẫn đến việc áp dụng các định luật bảo toàn đưa kết quả sai như bảo toàn mol electron, bảo toàn điện tích, bảo toàn khối lượng hay bảo toàn nguyên tố.
Vì vậy, trong dạng bài này, học sinh nên biết được rằng sẽ có mặt của NH4NO3.
=> Chuẩn bị kỹ năng suy luận, phán đoán bằng cách luyện tập thật nhiều đề vận dụng cao.
Ban tư vấn tuyển sinh Trường Cao đẳng Y khoa Phạm Ngọc Thạch tổng hợp

TRƯỜNG CAO ĐẲNG Y KHOA PHẠM NGỌC THẠCH
![]() Địa chỉ: Số 127/3 - 5 Hoàng Hoa Thám, Phường Tân Bình, TP.Hồ Chí Minh
Địa chỉ: Số 127/3 - 5 Hoàng Hoa Thám, Phường Tân Bình, TP.Hồ Chí Minh
![]() Điện thoại / Zalo / Line: 0899 955 990 - 0969 955 990
Điện thoại / Zalo / Line: 0899 955 990 - 0969 955 990
- Website: caodangduoctphcm.org.vn
- Facebook: www.facebook.com/TruongCaoDangYKhoaPhamNgocThachTPHCM
 Các bài viết liên quan
Các bài viết liên quan

 Lỡ đăng ký xét tuyển sai, làm sao?
Lỡ đăng ký xét tuyển sai, làm sao?
 Chậm nhất vào ngày 1/8, các thí sinh sẽ nhận được giấy báo dự thi THPT
Chậm nhất vào ngày 1/8, các thí sinh sẽ nhận được giấy báo dự thi THPT
 Kỳ thi THPT 2020: Siết chặt kỷ luật trong phòng thi
Kỳ thi THPT 2020: Siết chặt kỷ luật trong phòng thi
 HOT: Nhiều ngành mới và phương thức tuyển sinh mới được áp dụng
HOT: Nhiều ngành mới và phương thức tuyển sinh mới được áp dụng
 Thông tin tổng quan về ngành Sư phạm Hóa học
Thông tin tổng quan về ngành Sư phạm Hóa học
 Ngành Kế toán hiện nay học trường nào tốt?
Ngành Kế toán hiện nay học trường nào tốt?
 Thông tin tuyển sinh ngành Tài chính Ngân hàng
Thông tin tuyển sinh ngành Tài chính Ngân hàng
 Quản trị nhân lực là gì? ngành quản trị nhân lực học ở trường nào?
Quản trị nhân lực là gì? ngành quản trị nhân lực học ở trường nào?
 Điểm chuẩn và các trường đào tạo ngành quan hệ quốc tế
Điểm chuẩn và các trường đào tạo ngành quan hệ quốc tế
-
 Danh sách mã các trường Đại học, Học viện và Cao đẳng 2024 92174 lượt xem
Danh sách mã các trường Đại học, Học viện và Cao đẳng 2024 92174 lượt xem
-
 Thuốc Alphachymotrypsin dùng để điều trị bệnh gì và cách dùng như thế nào? 91492 lượt xem
Thuốc Alphachymotrypsin dùng để điều trị bệnh gì và cách dùng như thế nào? 91492 lượt xem
-
 Giải đáp thắc mắc ngành Y thi khối nào? 78394 lượt xem
Giải đáp thắc mắc ngành Y thi khối nào? 78394 lượt xem
-
 Cuba vừa tìm ra vắc xin phòng bệnh ung thư phổi đầu tiên trên thế giới 76502 lượt xem
Cuba vừa tìm ra vắc xin phòng bệnh ung thư phổi đầu tiên trên thế giới 76502 lượt xem
-
 Tiến sĩ Y khoa ĐH Mỹ chứng minh BS Lương vô tội 74573 lượt xem
Tiến sĩ Y khoa ĐH Mỹ chứng minh BS Lương vô tội 74573 lượt xem
-
 Thuốc Brawn Omeprazole là gì? Công dụng, liều dùng như thế nào? 59739 lượt xem
Thuốc Brawn Omeprazole là gì? Công dụng, liều dùng như thế nào? 59739 lượt xem
Website chính thức của Trường cao đẳng y khoa Phạm Ngọc Thạch, mọi thông tin sao chép cần được đồng ý bằng văn bản.





